Из всех компонентов, которые присутствуют в смартфоне, больше всего слухов и разных мнений существует вокруг аккумулятора. Кто-то говорит, что обязательно нужно регулярно заряжать и разряжать батарею в ноль, кто-то опасается ставить батарею на зарядку на всю ночь.
В этой статье я расскажу, как именно работает аккумулятор в современных смартфонах, откуда там появляется ток, почему происходит потеря емкости со временем, как лучше заряжать/разряжать ваш гаджет и почему батарея может взорваться.
Электроны, протоны, нейтроны
Начнем с теории, как это устроено. Большинство людей представляет схему работы аккумулятора в виде сосуда, в который заливается ток, а потом в течение дня мы начинаем его расходовать для питания смартфона или другого электронного прибора. Заряд закончился, аккумулятор сел, и нужно заполнить сосуд заново.

Но на деле батарея больше похожа на песочные часы, только наполнены они не песком, а электронами. И когда в верхней части электроны заканчиваются, то зарядка как бы переворачивает часы и пересыпает электроны из нижней части обратно в верхнюю.
Только в классических часах песок перемещается под действием силы тяжести, а чтобы понять, почему электроны переходят из одной части часов в другую, вспомним вообще, что такое электроны.
Окружающий мир состоит из атомов, атомы состоят из электронов и ядра, а ядро состоит из протонов и нейтронов. Электроны образуют электронные оболочки атомов с отрицательным зарядом, протоны имеют положительный заряд, а нейтроны нейтрально заряжены.
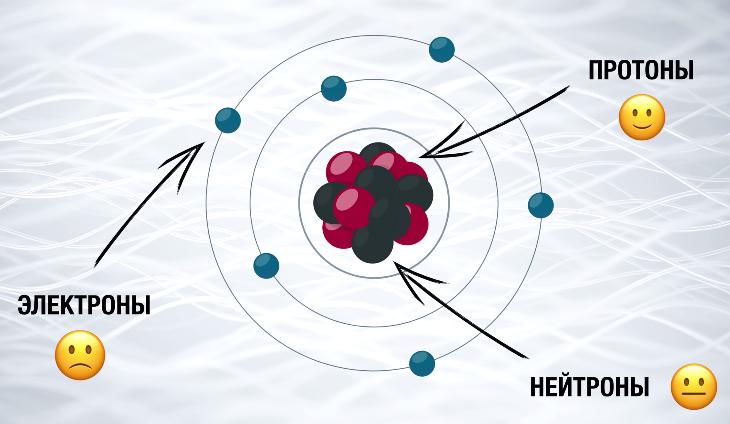
Если количество электронов и протонов одинаковое, то атом считается нейтральным. В атоме может быть больше электронов или протонов, тогда атом будет обладать отрицательным (Анион) или положительным (катион) зарядом.
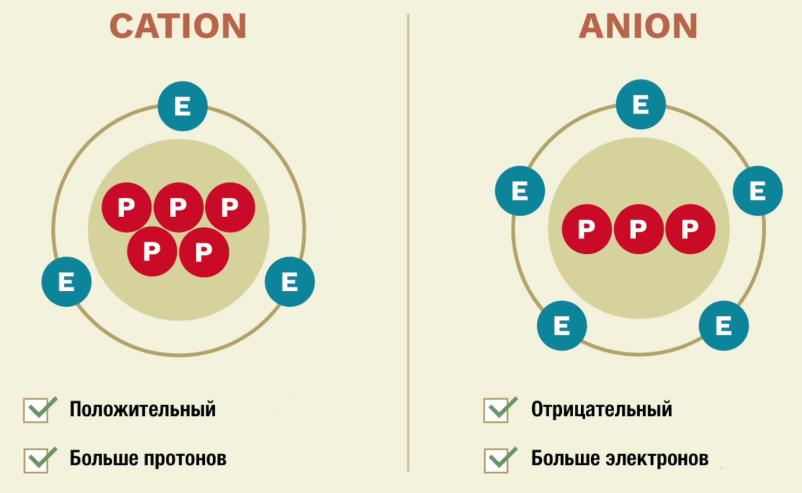
Отрицательные и положительные заряды всегда притягиваются друг другу, а одинаковые заряды отталкиваются. И атомы всегда стремятся стать нейтральными.
Если мы возьмем наши песочные часы и разделим их: в одной части разместим отрицательные электроны, а в другой части положительные ионы (где мало электронов), а потом соединим проводом две части часов, то электроны побегут соединяться с ионами создадут тем самым электрический ток.
В нашей ситуации этим “проводом” будут являться компоненты смартфона, такие как плата, экран камеры и прочее. А “песочными часами” выступает сам аккумулятор с плюсом и минусом.

Когда все электроны перешли от минуса к плюсу, и атомы стали нейтральны, наш аккумулятор собственно и разрядился. А чтобы зарядить его опять, нам требуется повторить весь процесс в обратном порядке. То есть заставить электроны вернутся обратно в одну из частей песочных часов.
Из аккумулятора электроны не расходуются окончательно, и зарядное устройство не наполняет его новыми. Мы просто разделяем все это и перемещаем обратно.
Литий-ионные аккумуляторы
В большинстве смартфонов установлены литий-ионные батареи – это самый популярный тип аккумуляторов в электронных устройствах, в том числе бытовой техники и электромобилях.
Литий-ионный аккумулятор состоит из двух частей: одна из них будет отрицательной (анод), а вторая положительной (катод).
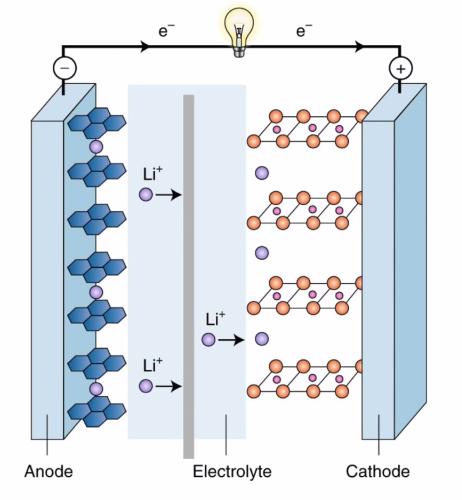
В Аноде используются ионы лития, а катоды чаще всего изготавливают из кобальта. Литий, простыми словами, “очень нервный товарищ” и легко вступает в реакцию. И эту реакцию очень легко вызвать.
Он имеет один электрон на внешней оболочке и легко может его потерять, превратившись из отрицательного в положительно заряженный ион.
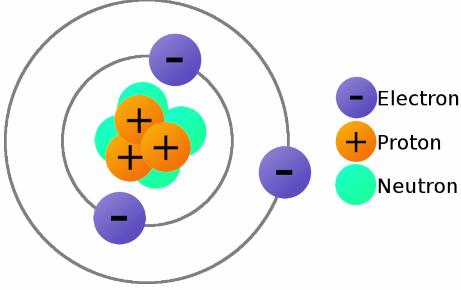
Но как только атом лития вступает в реакцию с оксидом металла, то становится стабильным. То есть к этой стабильности он постоянно стремится, от этого собственно он такой и нервный.
Для этого используется оксид кобальта, чтобы к нему притянулись электроны литья, и сами ионы лития наконец “успокоились”.
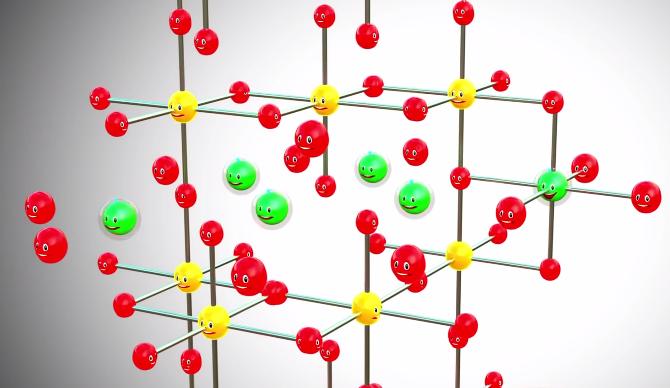
Но между анодом и катодом находится разделитель – жидкий электролит, который мешает отрицательным электронам лития напрямую попасть в положительный катод. Современные аккумуляторы используют разделитель из полимеров, пропитанных жидким электролитом, но суть работы это не меняет.
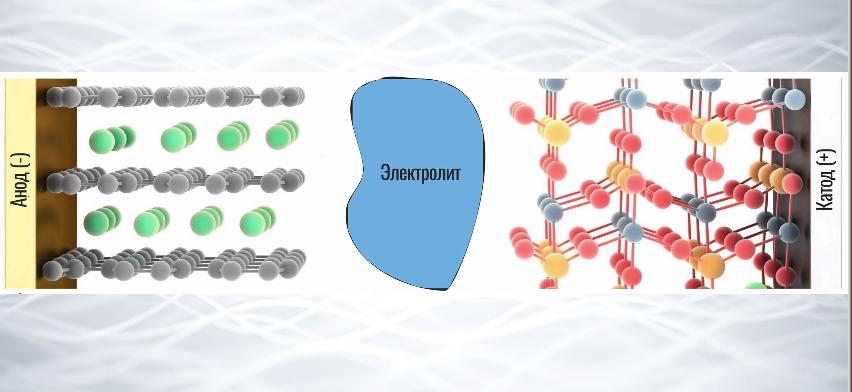
Электролит – это что-то типа контролера, который пропускает только положительные ионы лития, а отрицательные его электроны отправляет через компоненты нашего смартфона. На схеме можно увидеть, что в аноде ионы лития размещаются между слоями графита. Сам графит не вступает в реакцию, он просто служит своеобразным “шкафом с полками”, на которых можно удобно разместить ионы.
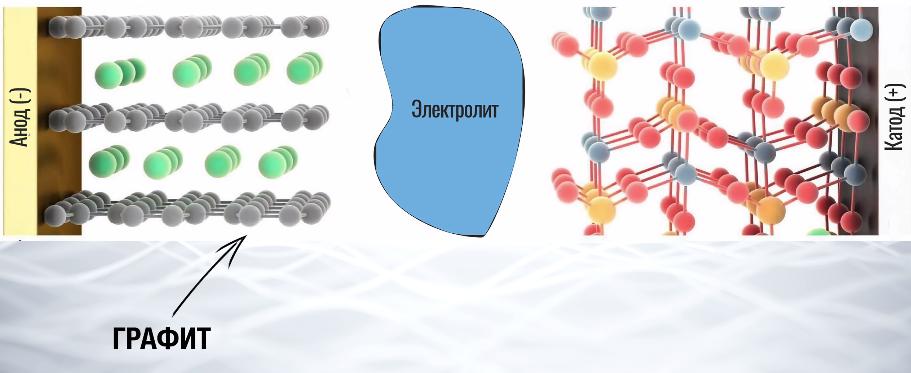
А в катоде находится оксид кобальта, который ждет и мечтает, как бы вступить в реакцию с положительно заряженным литием.
Что происходит при разрядке и зарядке аккумулятора? Как мы выяснили, с одной стороны у нас есть положительные атомы кобальта, которые хотят встретиться с электронами, с другой стороны у нас есть атомы лития, которые хотят отдать кобальту один свой электрон, пройти через электролит и соединиться с кобальтом, чтобы стать стабильным и спокойным товарищем.
Подключаем батарею к смартфону, и электроны отрываются от лития, проходят через цепи питания нашего устройства и попадает прямиком к положительно заряженному катоду. А в это время электролит пропускает положительно заряженный литий для связи с оксидом кобальта.
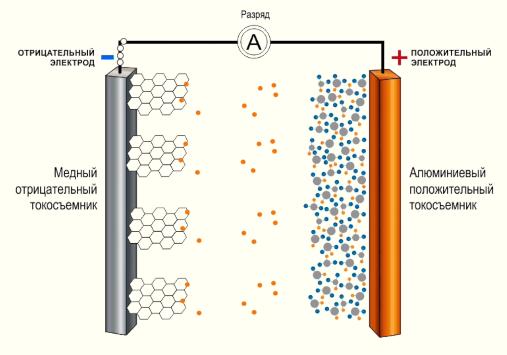
Ничего из нашего аккумулятора не уходит навсегда, а просто перемещается из одной части в другую. Для зарядки нам нужно вернуть все, как было. То есть с помощью внешнего адаптера питания с большим напряжением, чем в батарейке, мы вызываем химическую реакцию, и электроны отрываются от кобальта, и атомы лития тоже возвращаются в анод.
Так происходит полный цикл заряда и разряда.
Циклы батареи
Но технически понятие “циклы” введено исключительно для удобства. Все эти фишки с подсчетом циклов и емкости в настройках только для того, чтобы пользователю было проще ориентироваться в текущем состоянии батареи и ее оставшемся ресурсе.
Стандартный аккумулятор рассчитан на сохранение до 80% исходной емкости после 500 полных циклов зарядки при эксплуатации в нормальных условиях.
На самом деле, батарею убивает не производитель своими циклами, а сам процесс заряда и разряда. При любом сценарии эксплуатации рано или поздно вам потребуется заменить аккумулятор.
Как лучше заряжать
Потеря емкости происходит потому, что в путешествии через электролит не весь литий возвращается домой, часть его застревает на границе и потихоньку формирует барьер, через который рано или поздно литий не может переходить от анода к катоду и обратно.
На стороне катода тоже происходит реакция – окисление электролита. Это стать причиной вздутия аккумулятора из-за внутреннего накопления газов, вызванных окислением.

По этой причине аккумулятор постоянно держать заряженным и полностью разряженным не рекомендуется – это ускорит его деградацию и потерю емкости из-за формирования барьера между двумя частями аккумулятора.
Именно для этого в современных смартфонах есть опция Оптимизированной зарядки, когда ваш смартфон получит 80% заряда, потом понизит силу тока и будет потихонечку заряжаться до 100%.
В в любом современном смартфоне в аккумуляторе есть микросхемы, которые отвечают за заряд и разряд вашего гаджета. Они не позволят в обычном режиме эксплуатации выйти батарейки из строя раньше времени.

Если вы поставите ноутбук на зарядку и отключите через год, то есть очень большой шанс, что батарея будет держать уже далеко не так, как могла бы. Давайте аккумулятору работать – и все с ним будет в порядке.
Даже если вы будете заряжать его 5 раз в день от 40 до 70%, то это совершенно нормально.
Как лучше хранить
Рано или поздно батарею придется заменить, а если вам требуется какое-то время не пользоваться устройством, то рекомендуется зарядить батарею до 50%, выключить гаджет и хранить при комнатной температуре.
В таблице ниже видна прямая зависимость от уровня заряда и температуры хранения. Чем температура ниже, тем больше емкости останется.

Именно по этой причине новый телефон из коробки может показывать не 100% емкости, а например 99%. Выпускают смартфон задолго до того, как вы его купили, и некоторое химическое старение может происходить, пока устройство хранится в коробке в магазине.
Почему аккумуляторы взрываются?
В новостях периодически появляется информация о том, что смартфон на зарядке загорелся и ничего хорошего не произошло. Но технически загорается не смартфон, а именно батарея. Так в чем причина?
Есть два способа заставить взорваться литиевый аккумулятор: перегрев и физическое повреждение.
В процессе зарядки что-то может пойти не так, и поступающие напряжение продолжит поддерживать химическую реакцию. Один участок батареи становится слишком горячим, а поскольку зарядка продолжается, он не может охладиться и происходит то, что называется “тепловым разгоном аккумулятора”.

Горячий электролит нагревает все компоненты батарейки, образуется газ, который поднимает давление до тех пор, пока не трескаются корпус аккумулятора. А что происходит потом, я думаю, многие видели в интернете.

Но современные аккумуляторы имеет крайне малый процент отказов из-за теплового разгона. Производители применяют различные меры безопасности, типа негорючих добавок в электролит и так далее.
Вторая причина – это физическое повреждение изоляции батареи. Если сильно повредить корпус аккумулятора, катод с анодом сомкнутся, и может возникнуть возгорание. Во всех случаях соединения катода с анодом возникает короткое замыкание, нагрев и разложение электролита. После чего в самом лучшем случае происходит испарение этого электролита.
Не стоит пытаться самостоятельно разобрать или разрезать батарейку. Замыкание инородным предметом может привести к моментальному взрыву.
Из рекомендаций: старайтесь не ронять и не кидать смартфон, не пытайтесь его согнуть, не топите и не держите на солнце выше 50 градусов, не заряжайте китайскими блоками питания.





